DNA G-四链体(G4s)是一种由连续的富含鸟嘌呤的DNA序列形成的四重螺旋结构。尽管人们认为DNA G4s参与了各种生物过程,但由于缺乏合适的策略选择性地将DNA G4稳定在特定位点,因此在许多情况下,它们的致病作用在很大程度上尚不清楚。
7月3日,中国科学院长春应用化学研究所曲小刚教授及其同事在《自然细胞生物学》上发表的一项研究中提出了一种新策略,通过结合CRISPR和G4稳定蛋白或化合物来实现特定基因组位置的DNA G4s稳定。
研究人员利用成簇的规律间隔的短回文重复序列相关死Cas9(CRISPR/dCas9)靶向构建体,使G4稳定分子具有在不同G4中的选择性。并且dCas9/G4稳定分子复合物可以通过策略性的单向导RNA(sgRNA)设计来稳定基因组中的任何G4结构,而不会对活细胞中其他非靶向G4产生显著影响。
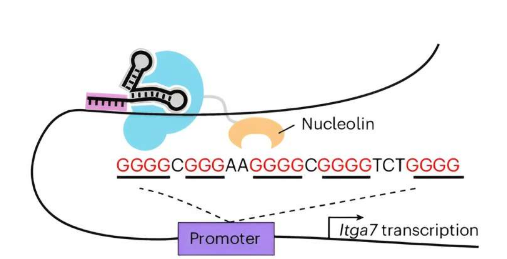
G4稳定蛋白核仁素与dCas9融合,可以特异性地稳定致癌基因MYC和肌肉相关基因Igta启动子中的G4以及端粒G4,分别导致细胞增殖停滞、成肌细胞分化受到抑制和细胞衰老。
此外,CRISPR 还可赋予 G4 结合化合物吡啶并二甲酰胺 (PDC) 和吡啶并噻唑 (PDS) 的 G4 内选择性。该策略已用于稳定两个已建立的 lncRNA NEAT1 和 MALAT1 启动子区内的 G4,以及与铁死亡、氧化应激、缺氧反应和 MAPK 通路有关的几个关键基因。
与传统的 G4 配体相比,CRISPR 引导的生物素结合 PDC 和 PDS 能够更精确地研究从头 G4 的生物学功能。
这一策略将为阐明特定 G4 与特定生物过程或人类疾病的关联铺平道路。此外,它还可能为在活细胞中筛选 G4 探针或 G4 候选药物开辟一条新途径,这些探针或候选药物仅针对感兴趣的 G4 具有特异性靶向性,且脱靶风险较低,从而促进基于 G4 的疾病诊断和治疗。
