科学家表明核糖体在血管形成中发挥着意想不到的作用
血管生成素是一种在细胞应激反应中起关键作用并有助于血管形成的酶,此前已发现它与实体癌肿瘤、神经退行性疾病和表观遗传的形成有关,四十年来一直是科学家深入研究的焦点。
马萨诸塞大学陈曾熙医学院的 Andrei Korostelev 博士和 Anna Loveland 博士的研究表明,核糖体通过激活血管生成素来裂解转移 RNA(tRNA),从而停止蛋白质的产生,在其功能中发挥着意想不到的作用。
该研究结果发表在《自然》杂志上,揭示了核糖体在血管生成功能中的独特作用,这可能对癌症治疗和神经退行性疾病治疗的设计具有重要意义。
“阐明血管生成素的功能和治疗潜力需要精确了解其激活所涉及的分子机制,”RNA 治疗学教授、研究作者 Korostelev 博士说。“我们的工作解答了关于血管生成素激活的一个长期问题。我们表明核糖体与酶结合并改变酶的形状,因此它可以裂解 tRNA。
Korostelev 补充道:“这些发现为转化研究打开了大门,有望探索针对血管生成素核糖体结合治疗癌症和神经退行性疾病的治疗潜力。”
血管生成素是一种切割 RNA 的核糖核酸酶,于 1985 年被鉴定为第一种已知的刺激血管生成(血管形成)的酶因子。这一发现在当时具有革命性,因为它支持了癌细胞促进血管生长以支持自身的理论,随后数十年对癌症治疗、伤口愈合、再生、器官发育和神经发育中的血管生成进行了研究。
尽管人们已经知道血管生成素可以通过切割细胞中的 tRNA 来抑制蛋白质合成,但实验室实验却发现纯化的血管生成素的切割活性水平非常低。这让研究人员感到困惑,他们无法确定血管生成素被激活的机制,导致一些人认为其他未识别的细胞成分在血管生成素激活中发挥了重要作用。
“血管生成素是决定脊椎动物血管形成的蛋白质,”RNA 治疗学助理教授、该研究的共同作者洛夫兰博士解释说。“当细胞受到压力和缺氧时,血管生成素就会被激活,形成新的血管来提供氧气。
“同样,癌细胞利用刺激血管生成素的机制来形成新血管,然后这些新血管可以为肿瘤提供营养。在大脑中,血管生成素已被证明具有神经保护作用。例如,血管生成素的突变与肌萎缩侧索硬化症有关。
“尽管血管生成素具有根本的生物学重要性且已被深入研究,但直到现在,科学家们还无法确定血管生成素是如何被激活的。”
Korostelev 和 Loveland 正在利用最新的低温电子显微镜技术研究核糖体的结构,这时他们开始观察从他们的合作者 Allan Jacobson 博士实验室获得的核糖体样本中的未识别蛋白质。Allan Jacobson 博士是马萨诸塞大学陈曾熙分校微生物学和生理系统名誉教授和教授。
Cryo-EM 是一种电子显微镜技术,利用低温冷冻细胞样本,然后用电子束照射细胞样本。当电子穿过细胞样本时,会捕获图像,然后将其重建为高分辨率 3D 模型。
低温电子显微镜是研究生物分子结构不可或缺的工具,它使科学家能够以极其精细的水平观察生物分子的结构。
核糖体是细胞内的大型复杂机器。这些大分子机器通常负责蛋白质的合成。核糖体读取与基因遗传序列相对应的信使 RNA,并将氨基酸组装成产生特定蛋白质所需的顺序。
然而,根据科罗斯捷列夫和洛夫兰的说法,在压力之下,核糖体会发挥额外的、意想不到的作用。
“当我们查看核糖体的图像时,我们发现有些不对劲,”洛夫兰说。“有一种蛋白质与我们的核糖体结合,但我们无法解释——从它的形状和折叠方式来看,它很可能是一种核糖核酸酶。它类似于血管生成素。”
通过化学分析,洛夫兰证实了他们的猜测。在细胞受到压力时,核糖体会结合并激活血管生成素。
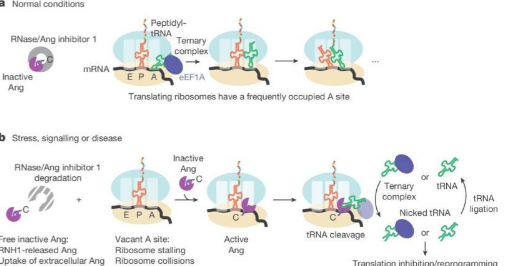
在无压力的情况下,血管生成素通常与抑制蛋白结合。与此同时,核糖体正忙于组装构建蛋白质所需的氨基酸。tRNA 将单个氨基酸带到核糖体的氨基酰基位点(A 位),在那里它与其他氨基酸结合产生蛋白质。
然而,在压力之下,情况就不同了。血管生成素与其抑制剂分离,翻译减慢,使核糖体的 A 位空置。血管生成素填补了这一空白,与 A 位结合并启动其核酸酶活性,使其能够切割下一个进入的 tRNA。这些切口会抑制 tRNA 功能和随后的蛋白质合成,最终调节多种细胞功能,例如血管形成。
Korostelev 表示:“这种裂解改变了基因向蛋白质的翻译。这些发现加深了我们对血管生成素如何被激活的理解,并提供了一个重要的新治疗靶点和后续效应供研究。”
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!
-
【木地板材料】木地板是一种广泛应用于家居和商业空间的地面装饰材料,因其自然美观、耐用性强、环保性好等特...浏览全文>>
-
【木地板安装】木地板安装是一项需要细致规划和专业操作的工程,无论是新房装修还是旧房翻新,选择合适的木地...浏览全文>>
-
【木的组词怎么写】在汉语学习中,词语的积累和运用是非常重要的部分。对于“木”这个字来说,它不仅是常见的...浏览全文>>
-
【木的象形字有哪些字】在汉字的发展过程中,许多字最初都是通过象形的方式创造出来的,用来表示具体的事物。...浏览全文>>
-
【木岛法子介绍】木岛法子(Kazuko Kikuchi)是日本著名演员、模特及艺人,以其在影视作品中的出色表现和独特...浏览全文>>
-
【木代尔是什么面料】“木代尔是什么面料”是许多消费者在选购衣物时常常会提出的问题。木代尔是一种天然纤维...浏览全文>>
-
【木代尔和莫代尔哪种面料好】在选择衣物面料时,很多人会遇到“木代尔”和“莫代尔”这两个名称,容易混淆它...浏览全文>>
-
【萝卜的营养价值】萝卜是一种常见的根茎类蔬菜,不仅味道清脆爽口,还具有丰富的营养价值。无论是生吃、炒食...浏览全文>>
-
【萝卜的药用功效和作用】萝卜,作为日常生活中常见的蔬菜之一,不仅味道清脆、营养丰富,还具有多种药用价值...浏览全文>>
-
【萝卜的家常做法】萝卜是一种非常常见的蔬菜,不仅价格实惠,而且营养丰富,适合多种烹饪方式。无论是炖、炒...浏览全文>>
