新模型揭示管状组织如何形成均匀的通道
日本理化学研究所的科学家开发出一种模型,可以解释细胞骨架有序排列的过程,而细胞骨架排列的过程正是管状结构网络形成的基础,这些管状结构为我们的身体提供生存所需的氧气和营养。这项研究发表在《自然通讯》上。
为了使血液稳定地流经循环系统,我们的血管需要保持均匀的内部通道,也称为管腔。这是通过用一种叫做肌动蛋白的蛋白质组成的规则间隔的环形电缆加固来实现的。类似的肌动蛋白结构还可以稳定连接大脑内神经元的细胞突起,以及形成果蝇呼吸系统的管状网络。
然而,人们对这些管状结构形成过程的了解仍然很少。“这些管状组织如何形成光滑、均匀的管腔,这真是一个谜,”理化学研究所生物系统动力学研究中心 (BDR) 的 Sayaka Sekine 说道。
为了探究这个问题,由 Sekine 和同样来自 BDR 的 Mitsusuke Tarama 领导的团队使用苍蝇呼吸系统气管的发育作为模型。
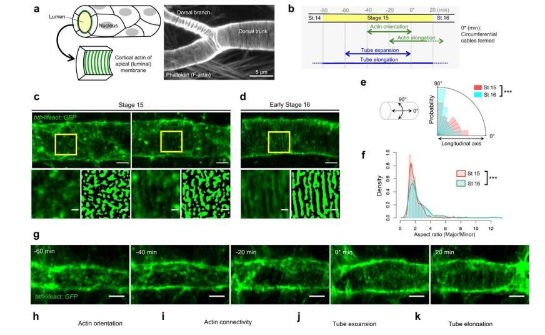
初步实验表明,在完全形成的小管中看到的管腔强化肌动蛋白索最初来自椭圆形的肌动蛋白组合,研究人员将其称为肌动蛋白纳米团簇。
为了确定有助于这些纳米团簇形成和组织的基因,研究小组系统地抑制了已知编码与肌动蛋白相互作用的蛋白质的 119 种基因。
基于这些实验和后续实验的见解,研究小组开发了肌动蛋白组装过程的计算机模型,其中他们将系统归结为少数几个变量。
“基本策略是使模型尽可能简单,但不要太简单,”Tarama 解释道。
他们的模型显示,当小管向外扩张时,应力的不均匀分布会诱发一种叫做凌乱相关形态发生激活剂 (DAAM) 的蛋白质的反应,进而促进肌动蛋白纳米团簇重新排列成管腔内有序排列、间距均匀的电缆。
Sekine 说:“从肌动蛋白纳米团簇到电缆形成的整个转变过程可以通过扩张小管中的自组织来解释。”
她和她的同事现在希望更好地掌握驱动这种肌动蛋白纤维组装的传感机制。“阐明详细的分子机制可能使更准确的计算机建模和预测其他管状组织中肌动蛋白的高级结构成为可能,”Sekine 说。
Sekine 指出,这些机制可能在更复杂的人体组织(包括原始心管)的形成过程中发挥作用。
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!
-
【木地板材料】木地板是一种广泛应用于家居和商业空间的地面装饰材料,因其自然美观、耐用性强、环保性好等特...浏览全文>>
-
【木地板安装】木地板安装是一项需要细致规划和专业操作的工程,无论是新房装修还是旧房翻新,选择合适的木地...浏览全文>>
-
【木的组词怎么写】在汉语学习中,词语的积累和运用是非常重要的部分。对于“木”这个字来说,它不仅是常见的...浏览全文>>
-
【木的象形字有哪些字】在汉字的发展过程中,许多字最初都是通过象形的方式创造出来的,用来表示具体的事物。...浏览全文>>
-
【木岛法子介绍】木岛法子(Kazuko Kikuchi)是日本著名演员、模特及艺人,以其在影视作品中的出色表现和独特...浏览全文>>
-
【木代尔是什么面料】“木代尔是什么面料”是许多消费者在选购衣物时常常会提出的问题。木代尔是一种天然纤维...浏览全文>>
-
【木代尔和莫代尔哪种面料好】在选择衣物面料时,很多人会遇到“木代尔”和“莫代尔”这两个名称,容易混淆它...浏览全文>>
-
【萝卜的营养价值】萝卜是一种常见的根茎类蔬菜,不仅味道清脆爽口,还具有丰富的营养价值。无论是生吃、炒食...浏览全文>>
-
【萝卜的药用功效和作用】萝卜,作为日常生活中常见的蔬菜之一,不仅味道清脆、营养丰富,还具有多种药用价值...浏览全文>>
-
【萝卜的家常做法】萝卜是一种非常常见的蔬菜,不仅价格实惠,而且营养丰富,适合多种烹饪方式。无论是炖、炒...浏览全文>>
